热点新闻
热点新闻
韩鸿宾团队提出细胞外间隙神经调控新理论,研发细胞外间隙分子转运调控新技术,在脑病治疗领域取得突破
近日,《中国科学:生命科学》杂志在线发表了北京大学韩鸿宾教授课题组的研究成果。
脑卒中是全球第二大死亡原因,也是导致国人死亡的首要杀手。近二十年来,韩鸿宾团队一直致力于经脑细胞外间隙(extracellular space,ECS)的脑重大疾病的诊疗研究。脑ECS占据着活体脑容积的15%~20%,远超过以往备受重视的脑血管所占据的3%~5%;ECS内分子转运与睡眠、记忆和感觉形成等脑功能活动密切相关。脑ECS不仅在脑病的发生、发展中起到重要作用,也是药物入脑实质后到达神经细胞靶点、发挥作用的必经通道。血脑屏障极大地阻碍了经血管途径的脑卒中新药研发。经脑ECS途径给药可有效避开血脑屏障,直接在脑内发挥作用,为脑病治疗提供了全新方向。
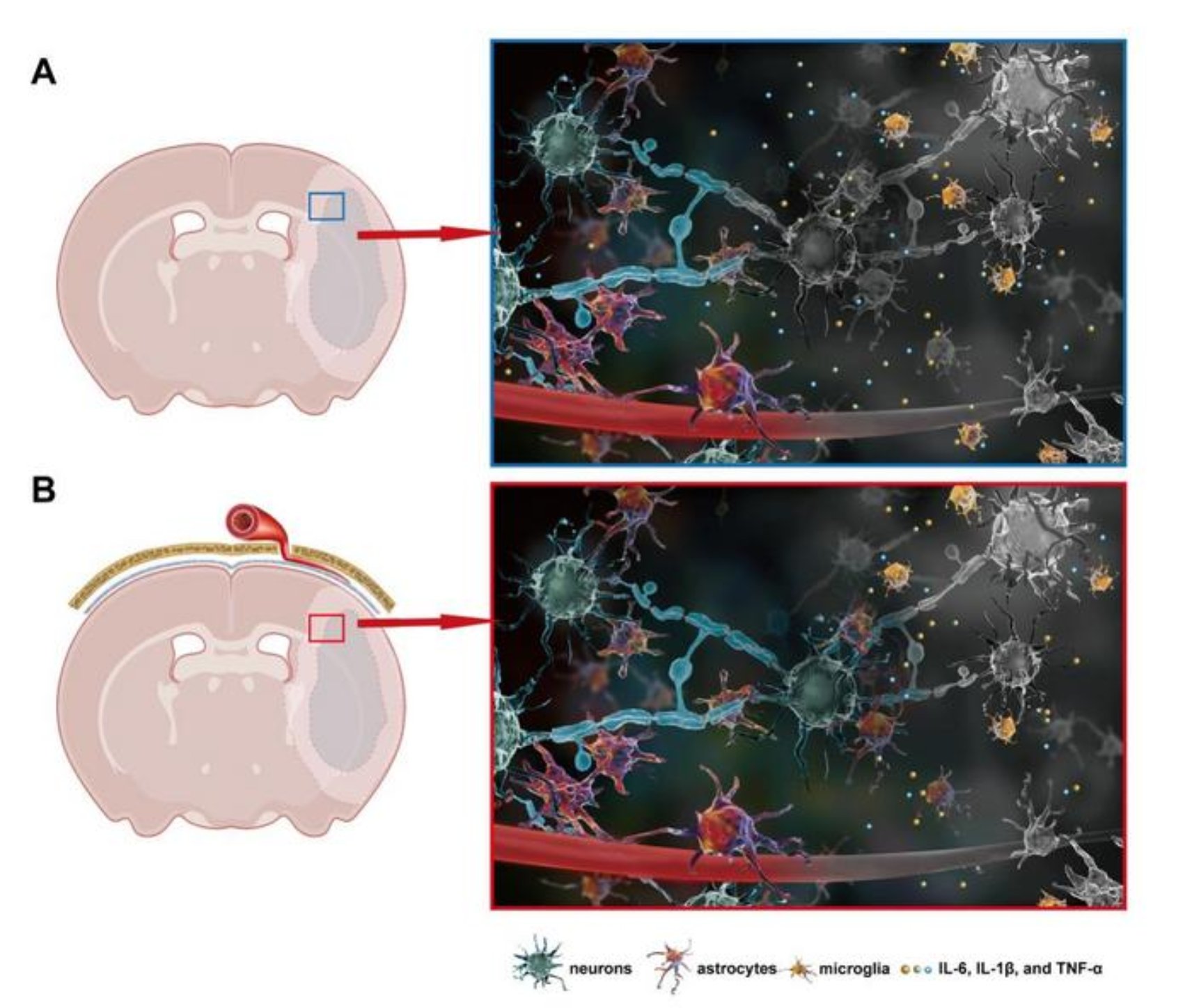
m-EAI治疗缺血性脑卒中的机制示意图
A. 脑卒中发生后,中枢神经系统中的各类细胞会发生不同的形态改变。梗死核心区神经元受影响最大,其细胞体和轴突消失,神经胶质细胞通常会出现细胞肿胀。缺血半暗带区神经元被称为 "缺血性神经元",相对来说还能存活,小胶质细胞和星形胶质细胞可转变为 "活化状态",同时产生促炎细胞因子。B. m-EAI术可以加快缺血半暗带区ISF引流,促进促炎细胞因子的清除,进一步减少胶质细胞的激活,从而挽救缺血半暗带区神经元。Credit: ©《中国科学》杂志社
十年前,团队就曾经在SCIENCE CHINA Life Sciences杂志发表研究论文,提出经脑ECS途径的新型给药技术-简单扩散给药(simple diffusion delivery, SDD)。该技术攻克了对流增强给药(convection enhanced delivery,CED)存在的药物逆流和精准定量分析困难两大技术瓶颈。研究发现,应用SDD方法,仅用传统给药方法1/800的神经药物胞二磷胆碱的药量,就实现超过6倍的缺血区神经保护范围,这也是首次证实经ECS途径微创给药治疗缺血性脑卒中的可能性和有效性。由于SDD和CED均是有创性给药,因此解决该方法有创性是实现临床转化实际应用的关键。
团队经过13年的科技攻关,最终解决了这一技术难题,提出并建立了微创、安全的改良型硬膜外动脉贴敷术(modified epidural artery implantation,m-EAI)。在之前的研究中,团队已经证实了EAI术对脑ECS内组织间液(interstitial fluid,ISF)引流的加速作用。在本研究中,再次证实了改良EAI术(m-EAI)的脑组织液引流加速作用,并且,改良法实现了在缺血后的不同时间点启用EAI,实现对ISF引流加速作用的动态控制。新方法不仅无需穿刺破坏硬脑膜,并且提供了和SDD相同的神经保护效果。研究证实,这种神经保护作用是通过减少在脑ECS内的IL-6、IL-1β和TNF-α等促炎细胞因子的蓄积实现的,ISF引流加速不仅在减少缺血区局部炎症反应,也同时减缓了小胶质细胞和星形胶质细胞的过度活化。
综上所述,该研究提出了通过调节ECS分子转运来治疗缺血性脑卒中的新方法。特别值得注意的是,这种微创方法是在不使用任何神经保护药物的情况下实现的缺血区神经保护作用,因此,联合使用m-EAI和神经保护药物对缺血性脑卒中的神经保护作用效果的研究特别值得期待。同时,该研究也验证了炎症反应是加剧中风缺血区神经损伤的理论假说。
研究详情请见原文:
A novel neuroprotective method against ischemic stroke by accelerating the drainage of brain interstitial fluid(http://engine.scichina.com/doi/10.1007/s11427-024-2592-4)


