热点新闻
热点新闻
基于细胞外间隙分区理论的神经调控新技术在脑病治疗研究中取得新进展
近日,机器人领域全球排名前三的《Cyborg and Bionic Systems》杂志连续报道了北京大学韩鸿宾团队关于经细胞外间隙(Extracellular Space,ECS)途径的神经调控新理论、新技术最新研究成果,分别为帕金森病和缺血性脑卒中相关研究。脑细胞外间隙为大脑活动提供了基本条件和空间微环境,在脑部疾病发生、发展及转归过程中发挥着至关重要作用。近年来,随着细胞外间隙内分子转运主动调控技术的成功实现,构建经全新途径神经调控和脑病治疗的理论和技术体系已突破在即。


本次报道的两篇研究成果分别聚焦于帕金森病和脑卒中两大危害人群的重大脑病。丘脑底核-脑深部电刺激(STN-DBS)对黑质区多巴胺能神经元的保护作用及其潜在机制尚未被充分阐释,导致调控效果不稳。该研究应用课题组自主研发的细胞外间隙成像探测仪,明确了STN-DBS对黑质区ECS和细胞外基质(ECM)改变以及邻近水通道蛋白4(AQP-4)表达的作用及其规律,阐释了DBS对黑质区微环境进行干预作用的远程调控机制(图1)。研究为解决DBS治疗异质性难题提供全新思路。脑卒中是全球第二大死亡原因,也是我国居民的首要致死疾病。传统血管途径给药需突破血脑屏障限制,而经脑ECS途径给药可绕过阻碍药物入脑的血脑屏障,为脑病治疗提供全新途径。2011年,韩鸿宾团队在Science China Life Sciences杂志曾报道了经细胞外间隙的简单扩散给药技术,解决了美方压力驱动给药导致的药物逆流难题,仅应用了传统给血管途径给药1/800的剂量即可实现6倍以上的缺血面积保护疗效。本次报道的研究重点解决了经ECS途径给药治疗的有创难题。在本次报道了应用755nm近红外光在硬膜外微创干预作用,可有效加速缺血再灌注损伤模型半暗带区ECS分子扩散速率约20%,并显著促进脑间质液(ISF)引流速度约40%,物质转运的加速减少了缺血局部的炎症因子(如IL-6、IL-1β和TNF-α)以及神经病理蛋白(如tau、p-tau和Aβ)沉积,从而减轻脑组织损伤并改善认知功能(图2)。
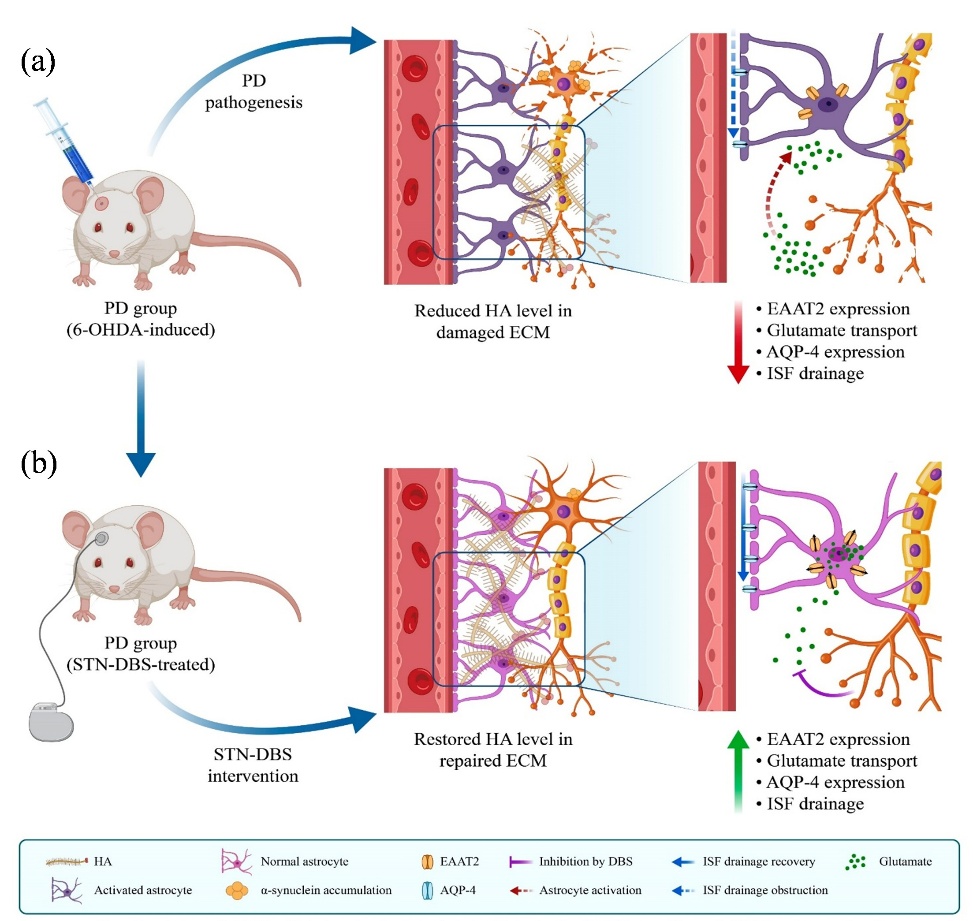
图1: STN受电刺激后,PD大鼠模型黑质区细胞外间隙变化情况示意图
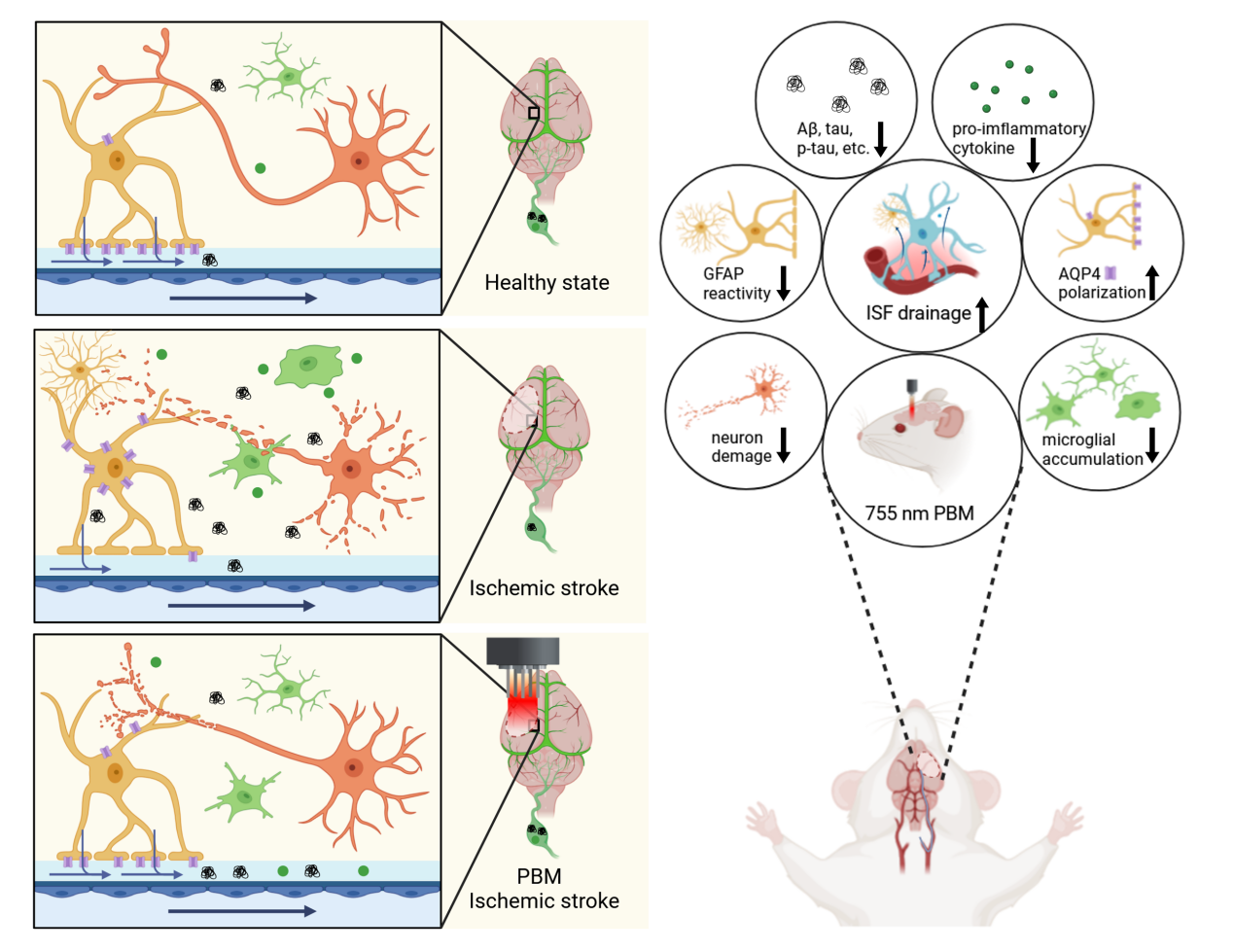
图2 755 nm的PBM用于缺血性卒中治疗的示意图
经ECS途径神经调控治疗帕金森病的机制研究报道的第一作者北京大学第三临床医学院在职博士杜丹,研究由清华大学医学工程技术专家付婉怡、北医三院神经内科专家傅瑜和航天中心医院神经外科专家尹丰共同完成。经ECS途径神经调控治疗缺血性脑卒中研究的第一作者北京大学第三医院影像医学与核医学博士杨柳,共同第一作者为北京大学第三医院放射科医师高亚娟,北京儿童医院放射科主任彭芸教授、北京大学医学技术研究院刘欣雨研究员为该文共同通讯作者。以上研究均由韩鸿宾教授作为首席的国家自然学基金委重大项目资助完成。
原文链接:
-帕金森病: https://doi.org/10.34133/cbsystems.0218
-缺血性脑卒中: https://doi.org/10.34133/cbsystems.0262


